Quelques-uns des principaux sujets de Géoforum

▲ Bourse minéraux et fossiles de Sainte Marie aux Mines (Alsace) - 24>28 juin 2026 ▲ |
-
Compteur de contenus
2900 -
Inscription
-
Dernière visite
Type de contenu
Profils
Forums
Galerie
Blogs
Boutique
Tout ce qui a été posté par phoscorite
-

Cavités et minéralogie secondaire dans les scories métallurgiques
phoscorite a répondu à un sujet de phoscorite dans Roche et pétrographie
... l'araldite teintée de bleu dont on se sert pour consolider la préparation (un sable) avant de scier et de faire la lame mince. Les analyses montrent aussi que le laitier altéré est hydraté (le total s'effondre) qu'il est très appauvri en S (d’où le sulfate néoformé) et aussi très enrichi en Mn, ce qui m'a beaucoup surpris, et si quelqu'un a des suggestions, surtout qu'il ne se prive pas... Si/Al est autour de 5 pour moi, avec les réserves qui s'imposent du fait que le programme de correction ZAF de la sonde doit être hors des clous avec un total aussi bas. Ça ne correspond à aucun silicate de ma connaissance, zéolite ou autre, et pourtant ça a l'air parfaitement bien cristallisé jusqu'au contact avec le laitier, même si on dirait que la microporosité de la moquette varie pas mal. Les totaux très bas sont peut-être liés à l'hydratation, mais certainement aussi à la microporosité, les cristaux sont bien plus petits que le bulbe d'analyse de la sonde. J'aurais bien aimé trouver une phase silicatée crédible pour ces tablettes en nid d'abeille et j'ai un peu de mal a voir deux minéraux dans cette moquette, mais cette suggestion est bien meilleure que pas d'explication du tout. La répartition de la moquette suggère que c'est un précipité en croissance externe sur le laitier altéré plutôt qu'une couche externe lessivée de ce laitier. La moquette n'existe que la ou le laitier est altéré (remarque judicieuse de @mr42) et elle est bien en surcroissance par rapport à l'ancienne limite du grain. -

Cavités et minéralogie secondaire dans les scories métallurgiques
phoscorite a répondu à un sujet de phoscorite dans Roche et pétrographie
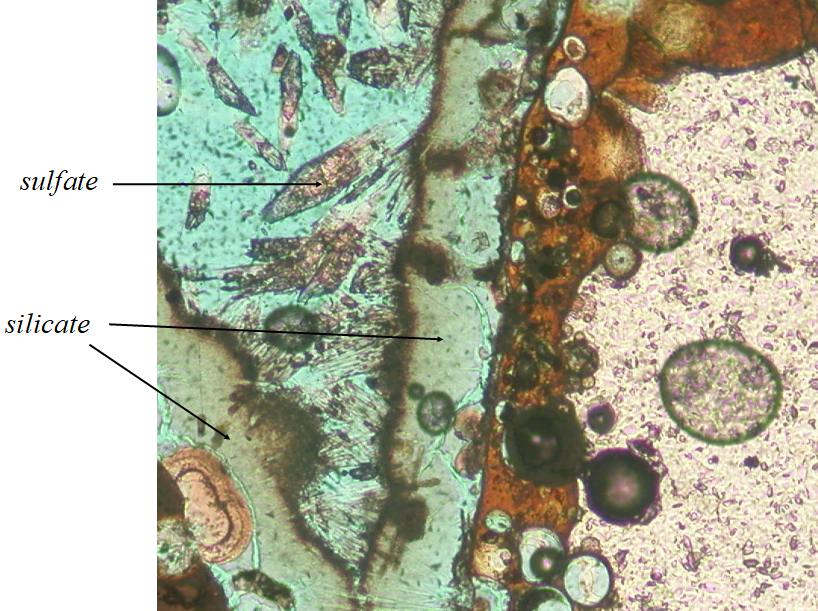
Bonsoir. Nous en avions un peu discuté en direct, Vous aviez évoqué la possibilité d'un procédé Martin. Voici en PJ les analyses ponctuelles dont je dispose pour la partie vitreuse (non altérée) et les parties altérées Pour les lames minces de ce matériel, voir les exemples ci-dessous. Les grains de laitier font un millimètre environ Une bulle et ses inclusions Un détail de la chemise (moquette) de silicate autour des grains altérés Laitiers_Grillet.xls -

Pierre verte du Valgaudemar, serpentine?
phoscorite a répondu à un sujet de trilobite05 dans Demandes d' identification de minéraux
Merci. Pour ma part, j'ai eu beaucoup de difficulté à voir quelque chose qui ressemblerait a un grenat dans votre photo, mais par contre il me semblait voir des quartz (gris). Et je renouvelle ma demande d'une autre photo de détail sur la face sciée. -

Cavités et minéralogie secondaire dans les scories métallurgiques
phoscorite a répondu à un sujet de phoscorite dans Roche et pétrographie
Non, désolé, plus maintenant. -

Dépôt de poussières atmosphériques sur le sol
phoscorite a répondu à un sujet de Christophe Reuss dans Géomorphologie, pédologie et géologie du quaternaire
Il existe un enregistreur naturel de ce type : les tourbieres, et l'enregistrement peut remonter assez loin dans le passé holocene... Voici une reference issue d'un labo de l'Université St-Etienne specialisé sur cette question. https://www.persee.fr/doc/bspf_0249-7638_2017_num_114_4_14837 -

Cavités et minéralogie secondaire dans les scories métallurgiques
phoscorite a répondu à un sujet de phoscorite dans Roche et pétrographie
OK, merci. J'ai retrouvé les quelques analyses faites a la microsonde de Clermont sur une lame mince de ce même morceau. C'est dans le fichier joint, qui contient aussi les analyses des sulfates. Les totaux sont très faibles, car le silicate est tres microporeux, mais le rapport Si/Al a l'air assez bien représentatif. Pour K, Ca et peut-être Mg, il y en a un peu mais c'est très variable. Du coup, je cherche maintenant du coté des zéolites, mais cet habitus en tablettes ne me dit rien du tout. Mineraux_Grillet.xls -

Cavités et minéralogie secondaire dans les scories métallurgiques
phoscorite a répondu à un sujet de phoscorite dans Roche et pétrographie
Dans ce mode d'observation, on privilégie la profondeur de champ et ne voit que la morphologie des cristaux. -

Cavités et minéralogie secondaire dans les scories métallurgiques
phoscorite a posté un sujet dans Roche et pétrographie
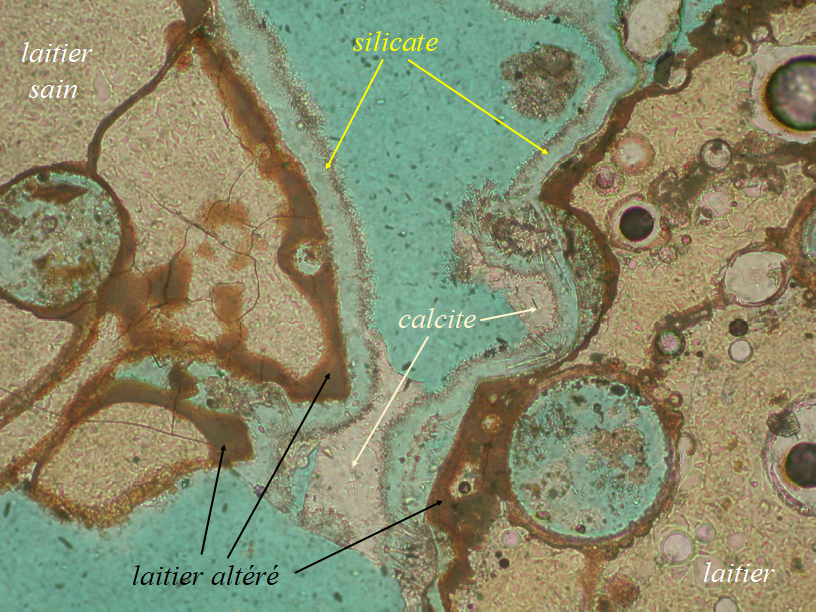
Salutations dominicales Les laitiers sont comme les basaltes : bourrés de cavités, basiques et instables dans les conditions de surface. Rien d'étonnant qu'ils s'altèrent et forment des minéraux secondaires. Leur étude est souvent orientée vers la compréhension des relargages indésirables en direction des nappes phréatiques, mais ces micro milieux peuvent aussi être assez plaisants à regarder de près. Je ne pratique pas la microminéralogie, mais pour vous donner envie de suivre ce petit filon, en voici un exemple (en noir et blanc) examiné au MEB. Les scories en question viennent d'un site proche de la ville de Firminy, @mr42connait, bien entendu. Les laitiers ont été granulés, ce qui donne à l'affleurement un aspect de sable gris. La partie haute du banc est cémentée (durcie) par le carbonate cristallisé entre les grains de laitier. C'est dans les pores entre ces grains, et/ou dans les bulles des grains de laitier altérés, que l'on va trouver les minéraux secondaires. Une cavité tapissée de calcite Une autre, avec un remplissage plus compliqué et des zonations de croissance (saisonnière ?) dans la calcite Plein de minéraux en aiguilles, formant des gerbes de plaquettes et/ou des fibres, en EDS, j'ai trouvé Ca, Al et S, donc de l'ettringite très probablement. . Dans ceux que j'ai sondés en Et puis il y a ce silicate mystérieux que je ne suis pas parvenu à identifier et qui forme une moquette sur le laitier altéré (visible à gauche de la deuxième photo et de la suivante, sur une sorte de coupe de la moquette) A l'époque j'avais pris ça pour de la brucite sans y regarder de près, mais les spectres EDS sont formels : beaucoup de Si, un peu d'Al, un tout petit peu de K, et rien d'autre (pas de Mg, ni de Fe, ni de Ca). La texture en nid d'abeille rappelle vaguement celle de chlorites diagenétiques, mais la, ce serait plutôt une illite anormalement riche en Si d’après la chimie. Je suis preneur si vous avez des idées sur ce que ça peut être. (NB: je n'ai pas de données DRX sur ces minéraux, seulement de la chimie ponctuelle). -
fluorescence X, c'est très différent. C'est une technique d'analyse chimique. On utilise aussi des rayons X pour bombarder la préparation (pastille pressée ou perle), mais cette fois on analyse les rayons X secondaires réémis par l’échantillon. Ces derniers dépendent du contenu chimique, pas du contenu cristallographique de l'échantillon. Par exemple, on aura la même réponse pour calcite et aragonite, pour quartz/tridymite/cristobalite, alors qu'en DRX on va les distinguer les uns des autres.
-
DRX = Diffraction des Rayons X : méthode qui permet d'analyser le réseau cristallin des minéraux. On travaille sur poudre (roche broyée) posée sur une lame que l'on fait tourner face à un faisceau X de longueur d'onde fixe. Sur un collecteur qui tourne autour du même axe, mais à une vitesse angulaire double, on enregistre un spectre de raies correspondant à des angles de diffraction, qui sont reliees simplement aux distances entre plans interatomiques des cristaux. Chaque minéral a un spectre de raies qui lui est propre. C'est compliqué pour les solutions solides. Les amorphes (verres, minéraux amorphisés) ne donnent pas de réponse. Pour la chondrite, je n'ai pas de photo, pas (encore) équipé, et je ne sais pas de quelle classe elle est. Échantillon récupéré par des collègues en mission australe, ils avaient gentiment proposé de faire plusieurs lames minces dans leur caillou...
-
Bonjour Dans l'expérience qui nous manque pour avancer par nous-mêmes sur ce caillou, il y aurait peut-être l'examen direct en microscopie de matériels qui ont été choqués de manière avérée. On pourrait espérer y apprendre en quoi c'est différent des roches magmatiques normales ou anthropiques sur lesquelles on a davantage de bagage. Sur les techniques à mettre en œuvre dans ce cas précis pour avancer, il y a la DRX, mais ça risquerait de nous amener à discuter surtout une paragenèse secondaire qui n'est pas vraiment ce que l'on a envie de comprendre. Pour la compréhension de la texture, et l'identification des éléments comme les bâtonnets, les prismes cariés ou les inclusions de la forme globuleuse, je préfèrerais largement une séance de MEB... Je ne suis pas sur de pouvoir négocier ça avec mon ancien labo de Saint-Étienne. Il m'est arrivé par le passé de fournir ce genre de service à des particuliers, mais l'utilisation des équipements est devenu très difficile hors activité contractuelle. Toulouse n'est pas très loin de chez moi, si c'est faisable, j'en suis. Je peux proposer plus facilement de regarder moi-même la lame mince avec mon propre micro polarisant, et de la renvoyer ensuite. Ça peut permettre de lever des incertitudes toujours présentes sur la préparation (épaisseur de la lame) qui compliquent l'examen indirect sur photos. Ce serait peut-être aussi l'occasion de commencer à échanger ou simplement faire circuler des lames minces pour ceux qui sont équipés de micros et qui souhaitent examiner de leurs propres yeux tel ou tel type de caillou déjà étudié. Pour amorcer, je propose d'envoyer (avec promesse de retour ou de relais vers un autre amateur du forum) une lame mince de chondrite ordinaire. Une adresse sur MP suffit.
-
Si c'est une roche transformée par des contraintes brutales, ou par un choc thermique, le problème c'est que presque toute notre expérience en pétrographie devient inopérante, voire contre-productive. On n'a simplement pas l'habitude d'en voir en lame mince, et on ne sait pas quelles observations il faudrait faire. Déja vu cette photo, et j'avais pensé a un artefact sans plus. Mais on peut aussi imaginer que le mineral (carbonate) contenait des inclusions fluides, et que suite a un choc thermique, celles-ci ont explosé...
-
Décidément, chaque prise de vue nous entraîne dans un nouveau monde... ce bleu "sodalite" est du plus bel effet. Dans la matrice microgrenue, on retrouve bien les contrastes déjà vus en lumière réfléchie sur l'échantillon scié, et on retombe sur les mêmes questions. Quels minéraux peuvent bien contenir du Fe là-dedans ? On ne voit rien qui ressemble à un oxyde ordinaire (magnétite, Ti-hématite, ilménite). Les minéraux les plus réfléchissants se trouvent bien (comme dans l'image MEB) entre les lattes de feldspath, mais aucun n'a un aspect métallique. On a l'impression que ce sont plus des minéraux qui diffusent bien la lumière (teintes laiteuses ou bleutées) que des oxydes métalliques standard. Même constat dans la forme globuleuse : les inclusions, pratiquement isotropes, sont bizarrement très lumineuses en LR. Ça ne peut pas être de la néphéline qui serait très sombre en LR; j'avais envisagé aussi des inclusions magmatiques (hypothèse pseudo-leucite) mais je ne vois pas pourquoi elles seraient bien plus réfléchissantes que le feldspath hôte... Le seul minéral de ma connaissance qui ressemble à ça serait de l'hercynite (spinelle riche en Fe), ce qui nous entrainerait vers une interprétation plus proche de la suggestion de @jjnom d'une roche ayant subi un choc physique ou thermique, et dans laquelle on ne reconnait plus les caractères optiques de certains minéraux pourtant courants.
-

Des roches étonnantes plus belles les unes que les autres... dans les Pyrénées
phoscorite a répondu à un sujet de triskell dans Roche et pétrographie
Bonjour Vous ne nous avez pas dit combien de specimens vous avez photographies, pour ma part, j'en vois trois. Un granite, avec sur un coté une cassure rainurée (miroir de faille très possible) Un leucogranite un peu déformé (ou orthogneiss leucocrate) avec un grain assez fin, beaucoup de muscovite et des formes en amandes à biotite+muscovite qui pourraient être d'anciennes cordiérites, voire d'anciens grenats. Un gneiss migmatitique (ou un orthogneiss) à grain beaucoup plus grossier, avec la aussi les ferromagnésiens regroupés en amandes, ce qui évoque toujours la rétromorphose d'un silicate d'Al. -
Dommage, sur le deuxième on reconnaissait assez bien l'un des éléments de la texture microgrenue, à savoir les lattes de feldspath de taille importante (200 microns). Et ce qui me trouble, c'est que dans l'image en électrons secondaires, le matériel interstitiel entre ces lattes apparait plus clair que les lattes elles-mêmes, ce qui veut dire que le numéro atomique moyen est plus élevé (ça contient des éléments plus lourds que le feldspath). Si j'avais vu cette photo sans voir les autres, j'aurais dit qu'on avait des lattes de plagioclase subautomorphe, avec du feldspath potassique (plus clair) interstitiel... Prendre l'avis de @BUTs'il est dispo, et peut-être aussi regarder en lumière réfléchie avec la polarisation, si votre microscope le permet. Si c'est possible, il faudrait regarder aussi les petits prismes roses cariés en lumière réfléchie, sur la lame mince. Bonne soirée
-

Pierre verte du Valgaudemar, serpentine?
phoscorite a répondu à un sujet de trilobite05 dans Demandes d' identification de minéraux
Bonjour Ça ressemble plutôt à une roche grenue à grain fin. Et il y a un peu trop de minéraux différents pour une serpentinite. Sur la surface sciée humide, en bas à droite, on devine deux baguettes vertes. Vous pourriez zoomer ? Et dans le haut de cette section, il y a deux objets verts en forme de lentilles un peu plus gros que le reste. Un autre zoom ? La dureté que vous indiquez est problématique, vous n'avez pas essayé de rayer autre chose avec ? -
Pas évident pour moi. Difficile d'avoir à la fois une section hexagonale et une section de triangle équilatéral. Pourquoi pas du cubique ? C'est toujours dans le même caillou ? Et tant que j'y suis, il y aurait d'autres clichés faits au MEB en électrons secondaires ?
-
C'est sympa d'envoyer des fleurs, mais il y a au moins une grosse incohérence dans le tableau récapitulatif que je viens d'envoyer, un peu trop vite. Comme vous l'avez remarqué sans doute, la roche est censée être assez riche en Fer, or dans ma liste de minéraux candidats pour la matrice microgrenue, il n'y a pratiquement aucun minéral riche en Fe qui soit suffisamment abondant. Le seul candidat possible dans ce bazar, ce sont les petits prismes roses en LR, et sombres en LPNA, qui ont l'air carriés. Ça ne peut donc pas être du sphène, mais plutôt un oxyde de Fe-Ti... Pourquoi faire compliqué ? C'est juste que les formes ne ressemblent pas a celles de la magnétite. Sur la deuxième photo MEB, on voit assez bien que la partie gauche du caillou est plutot grenue, alors que celle de droite est microgrenue. Et on avait déja cette impression dans les toutes premières photos, en voyant le bloc en entier. Une microsyenite avec des enclaves (autolithes) de syenite ? Bonne soirée
-
Merci @jean francois06 pour les liens et les références. Pour ma part, et par habitude, j'utilise "Optical determination of rock-forming minerals" de W.E. Troger. Si @zéoliteest d'accord, j'aimerais bien faire une tentative de synthèse de ce que l'on croit savoir sur ce caillou, avant de plier la boutique sur un échec. On a tout d'abord une idée (qualitative) de la composition chimique du caillou via un flash XRF qui donnerait : résultats bruts : Mg 6.5% Al 18.5% Si 56% Ti 2.6% Fe 18% Zr 0.09% Ca 2.4% K1.6% Après recalcul en oxydes et normalisation, la composition chimique donnerait ceci (Na2O, MnO et P2O5 sont arbitraires, juste pour la normalisation) SiO2 TiO2 Al2O3 Fe2O3 MnO MgO CaO Na2O K2O P2O5 57.6 2.1 16.8 12.4 0.0 5.2 1.6 3.0 0.9 0.3 100.00 avec Zr autour de 430 ppm. Pour une roche présumée subvolcanique, la richesse en Fe, Ti et Zr nous oriente vers une série alcaline, mais il y a quand même des anomalies (CaO trop bas par rapport à MgO, mais MgO est l'élement le plus leger qui soit évalué, donc le moins fiable pour ce type d'analyse) Maintenant le caillou. On y voit sur les tranches sciées et polies : - une matrice microgrenue - des phénocristaux - des OFNI (objets flottants non identifiés) tels que des amas de feldspaths de taille mm, et une forme globuleuse très bizarre. Dans la matrice, ci-dessous en Lumière Réfléchie (LR) On voit : - des baguettes blanc bleuté (petits plagioclases ?) englobés dans - des lattes un peu plus grosses, couleur crème (feldspath alcalin ?) - des petits prismes rosés avec pas mal de sections losangiques, et souvent cariés (partiellement dissous) - des interstices entre les feldspaths remplis d'un matériel jaunâtre - des petits oxydes (?) en aiguilles. Il faut s'accrocher pas mal pour retrouver ces divers types d'éléments quand on voit la lame mince en LPNA et LPA. Par exemple ici : On a l'impression que les petits prismes rosés à section losangique sont devenus des opaques (ou presque). Ce pourrait être du sphène... et que les bâtonnets blancs bleutés correspondent maintenant aux bâtonnets chagrinés avec des teintes roses et vertes en LPNA. Ça pourrait être une altération du plagio en saussurite. On reconnait plus facilement les feldspaths de plus grande taille (au centre) et le remplissage des interstices entre ces feldspaths qui prend des teintes entre rose et vert Pour les phénocristaux, à part les feldspaths de taille relativement grande, il semble qu'il n'y en ait qu'une seule catégorie : ils sont noirs en LR (sur la droite de la photo, on en voit plusieurs avec des formes nettes) Quand on passe à la lame mince, on voit qu'ils sont systématiquement altérés en produits fibreux, avec quelques carbonates. Après bien des hésitations et sur l'ensemble des exemples, mon interprétation la moins mauvaise est qu'il s'agirait, à l'origine, de néphélines, mais les produits d'altération sont assez atypiques (normalement, les argiles comme la montmorillonite sont incolores en LPNA alors qu'ici c'est entre rose et vert pale). En tout cas, ce n'est pas de la serpentine (teinte de polarisation trop haute) ce qui exclut olivine et opx/pigeonite comme phénocristaux. Reste la forme globuleuse, qui ne représente qu'une toute petite partie du caillou et dont l'interprétation (si on la connaissait) n’amènerait pas grand chose.
-
J'en aurais bien fait une amphibole alcaline (type kaersutite) mais il aurait fallu un angle < 20°... Avec ce pléochroïsme brun-rouge, une biréfringence modeste, ses macles et un angle d'extinction aussi fort, mes tables me proposent très peu de candidats. Je sèche...
-

identification 2 pierres fossiles ou simples pierres
phoscorite a répondu à un sujet de alkimik dans Forum Géologie
L'idée était que la concrétion s'était formée non pas sur un fossile, mais sur un noyau argileux un peu plus riche en matière organique que la marne hôte de la concrétion. D’où l'idée de galet mou (dépôt argileux partiellement induré puis resédimenté dans un écoulement gravitaire). Ce scénario situe le dépôt sur une pente, un peu instable, l'environnement paléogéographique usuel des slumps. Si vous pouvez couper et polir, regardez comment se fait le passage entre la croute et la mie (abrupt, progressif ?) et si vous voyez de grands cristaux dans la croute. Pour les concrétions, vous trouverez peut-être des éléments dans le papier de Selles en PJ (malheureusement, les photos ne passent pas) 1387277281_EarthSciRev1996_Selles_concretionclassification.pdf